Молекула бензола имеет строение правильного треугольника. Ароматические углеводороды. Бензол и его гомологи
ОПРЕДЕЛЕНИЕ
Ароматические углеводороды (арены) - вещества, в молекулах которых содержится одно или несколько бензольных колец.
Общая формула гомологического ряда бензола C n H 2 n -6 . Простейшими представителями ароматических углеводородов являются бензол - C 6 H 6 и толуол - C 6 H 5 -CH 3 . Углеводородные радикалы, полученные из аренов носят названия: C 6 H 5 - — фенил (Ph-) и C 6 H 5 -CH 2 — — бензил.
Первые члены гомологического ряда бензола - бесцветные жидкости со специфическим запахом. Они легче водды и в ней практически нерастворимы. Хорошо растворяются в органических растворителях и сами являются хорошими растворителями.
Электронное строение бензолов
Рассмотрим строение ароматических углеводородов на примере молекулы бензола. Это химическое соединение впервые было выделено из продуктов переработки каменного угля в 1825 году, однако, для того, чтобы установить строение его молекулы потребовалось три десятилетия. В 1865 году немец Ф. А. Кекуле высказал идею о том, что атомы углерода в бензоле соединены не в виде открытой цепи, а замкнуты в цикл (рис. 1). По его представлениям молекула бензола - это замкнутый цикл, состоящий из шести атомов углерода с тремя чередующимися двойными связями. Однако Кекуле так и не смог объяснить ряд особых свойств, присущих бензолу: почему бензол не проявляет склонность к реакциям присоединения (не обесцвечивает бромную воду и перманганат калия) несмотря на наличие двойных связей и т.д.
Рис. 1. Строение молекулы бензола по Кекуле.
Согласно представлениям современной органической химии, молекула бензола является правильным плоским шестиугольником. Все шесть атомов углерода находятся в sp 2 -гибридном состоянии. Каждый атом углерода образует σ - связи с двумя атомами углерода и одним атомом водорода, лежащими в плоскости цикла. Валентные углы между тремя σ - связями равны 120 o .
Каждый атом углерода в молекуле бензола имеет одну негибридизованнуюp - орбиталь. Шесть этих орбиталей располагаются перпендикулярно плоскому σ - скелету и параллельно друг другу. При их взаимном перекрывании образуется единое π-электронное облако, т.е. осуществляется круговая делокализация электронов. Наибольшая π-электронная плотность в этой сопряженной системе располагается над плоскостью σ - скелета молекулы и охватывает все шесть атомов углеродного цикла. В результате все связи между атомами углерода в бензоле выравнены и имеют длину 0,139 нм (рис. 2).

Рис. 2. Строение молекулы бензола.
Совокупность свойств бензола называют проявлением ароматического характера, или ароматичности. Явление ароматичности подчиняется правилу Хюккеля, согласно которому ароматические молекулы должны иметь плоский циклический σ - скелет и число обобщенных π-электронов, равное (4n+2), где n = 0, 1, 2, 3 и т.д.
Примеры решения задач
ПРИМЕР 1
| Задание | Плотность паров вещества 3,482 г/л. Его пиролиз дал 6 г сажи и 5,6 л водорода. Определите формулу этого вещества. |
| Решение | Сажа представляет собой углерод. Найдем количество вещества сажи исходя из условий задачи (молярная масса углерода равна 12 г/моль):
n(C) = m(C) / M(C); n(C) = 6 / 12 = 0,5 моль. Рассчитаем количество вещества водорода: n(H 2) = V(H 2) / V m ; n(H 2) = 5,6 / 22,4 = 0,25 моль. Значит, количество вещества одного атома водорода будет равно: n(H) = 2 × 0,25 = 0,5 моль. Обозначим количество атомов углерода в молекуле углеводорода за «х», а количество атомов водорода за «у», тогда соотношение этих атомов в молекуле: х: у = 0,5: 0,5 =1:1. Тогда простейшая формула углеводорода будет выражаться составом СН. Молекулярная масса молекулы состава СН равна: М(СН) = 13 г/моль Найдем молекулярную массу углеводорода исходя из условий задачи: M (C x H y) = ρ×V m ; M (C x H y) = 3,482×22,4 = 78 г/моль. Определим истинную формулу углеводорода: k= M(C x H y)/ М(СН)= 78/13 =6, следовательно, коэффициенты «х» и «у» нужно умножить на 6 и тогда формула углеводорода примет вид C 6 H 6 . Это бензол. |
| Ответ | Искомый углеводород имеет состав C 6 H 6 . Это бензол. |
Химическое строение
Атомы углерода в молекуле бензола образуют правильный плоский шестиугольник, хотя обычно его рисуют вытянутым.
Окончательно строение молекулы бензола подтверждено реакцией образования его из ацетилена. В структурной формуле изображается по три одинарных и три двойных чередующихся углерод-углеродных связей. Но такое изображение не передает истинного строения молекулы. В действительности углерод-углеродные связи в бензоле равноценны, и они обладают свойствами, не похожими на свойства ни одинарных, ни двойных связей. Эти особенности объясняются электронным строением молекулы бензола.
Электронное строение бензола
Каждый атом углерода в молекуле бензола находится в состоянии sp 2 -гибридизации. Он связан с двумя соседними атомами углерода и атомом водорода тремя у-связями. В результате образуется плоский шестиугольник: все шесть атомов углерода и все у-связи С--С и С--Н лежат в одной плоскости. Электронное облако четвертого электрона (р-электрона), не участвующего в гибридизации, имеет форму гантели и ориентировано перпендикулярно к плоскости бензольного кольца. Такие р-электронные облака соседних атомов углерода перекрываются над и под плоскостью кольца. В результате шесть р-электронов образуют общее электронное облако и единую химическую связь для всех атомов углерода. Две области большой электронной плоскости расположены по обе стороны плоскости у-связей.
p-Электронное облако обусловливает сокращение расстояния между атомами углерода. В молекуле бензола они одинаковы и равны 0,14 нм. В случае простой и двойной связи эти расстояния составили бы соответственно 0,154 и 0,134 нм. Значит, в молекуле бензола нет простых и двойных связей. Молекула бензола - устойчивый шестичленный цикл из одинаковых СН-групп, лежащих в одной плоскости. Все связи между атомами углерода в бензоле равноценны, чем и обусловлены характерные свойства бензольного ядра. Наиболее точно это отражает структурная формула бензола в виде правильного шестиугольника с окружностью внутри (I). (Окружность символизирует равноценность связей между атомами углерода.) Однако часто пользуются и формулой Кекуле с указанием двойных связей (II)
Ароматическими называются соединения, в молекуле которых имеется циклическая группа атомов с особым характером связи — ядро бензола. Международное название ароматических углеводородов — арены.
Простейшим представителем аренов является бензол С 6 Н 6 . Формула, отражающая строение молекулы бензола, была впервые предложена немецким химиком Кекуле (1865):
Атомы углерода в молекуле бензола образуют правильный плоский шестиугольник, хотя обычно его рисуют вытянутым.
Окончательно строение молекулы бензола подтверждено реакцией образования его из ацетилена. В структурной формуле изображается по три одинарных и три двойных чередующихся углерод-углеродных связей. Но такое изображение не передает истинного строения молекулы. В действительности углерод-углеродные связи в бензоле равноценны, и они обладают свойствами, не похожими на свойства ни одинарных, ни двойных связей. Эти особенности объясняются электронным строением молекулы бензола.
Электронное строение бензола.
Каждый атом углерода в молекуле бензола находится в состоянии />sp 2 -гибридизации. Он связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями. В результате образуется плоский шестиугольник: все шесть атомов углерода и все σ-связи С-С и С-Н лежат в одной плоскости. Электронное облако четвертого электрона (р-электрона), не участвующего в гибридизации, имеет форму гантели и ориентировано перпендикулярно к плоскости бензольного кольца. Такие р-электронные облака соседних атомов углерода перекрываются над и под плоскостью кольца 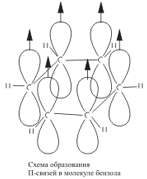 . В результате шесть р-электронов образуют общее электронное облако и единую химическую связь для всех атомов углерода. Две области большой электронной плоскости расположены по обе стороны плоскости σ-связей
. В результате шесть р-электронов образуют общее электронное облако и единую химическую связь для всех атомов углерода. Две области большой электронной плоскости расположены по обе стороны плоскости σ-связей  ./>/>
./>/>
p -Электронное облако обусловливает сокращение расстояния между атомами углерода. В молекуле бензола они одинаковы и равны 0,14 нм. В случае простой и двойной связи эти расстояния составили бы соответственно 0,154 и 0,134 нм. Значит, в молекуле бензола нет простых и двойных связей. Молекула бензола — устойчивый шестичленный цикл из одинаковых СН-групп, лежащих в одной плоскости. Все связи между атомами углерода в бензоле равноценны, чем и обусловлены характерные свойства бензольного ядра. Наиболее точно это отражает структурная формула бензола в виде правильного шестиугольника с окружностью внутри (I ). (Окружность символизирует равноценность связей между атомами углерода.) Однако часто пользуются и формулой Кекуле с указанием двойных связей (II
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
по курсу органической химии
«АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ »
Ростов-на-Дону
Методические указания по курсу органической химии «Ароматические углеводороды». - Ростов н/Д: Рост. гос. строит. ун-т, 2007. - 12 с.
Излагаются теоретические положения по теме “Ароматические углеводороды”. Дается определение ароматическим углеводородам, а также понятию “ароматичности”. Описывается строение молекулы бензола. Рассматривается номенклатура и изомерия ароматических соединений с одним бензольным ядром. Приведены основные методы получения аренов, также рассмотрены физические и химические свойства ароматических углеводородов.
Рассчитано на студентов I и II курсов дневной и заочной форм обучения специальностей ПСМ, ЗЧС, ССП, БТП и АС.
Составители: канд. хим. наук, доц.
М.Н. Мицкая,
канд. хим. наук, ассист.
Е.А. Левинская
Рецензент: канд. хим. наук, доц.
Л.М. Астахова
© Ростовский государственный
строительный университет, 2007
Ароматические соединения (арены) - органические соединения с плоской циклической структурой, в которой все углеродные атомы создают единую делокализованную π-электронную систему, содержащую (4n+2) π-электронов.
К ароматическим соединениям относятся прежде всего бензол С 6 Н 6 и его многочисленные гомологи и производные. Ароматические соединения могут содержать в молекуле одно или несколько бензольных ядер (многоядерные ароматические соединения). Но мы рассмотрим ароматические соединения с одним бензольным ядром.
Строение молекулы бензола
Бензол обнаружен М. Фарадеем в 1825 г. в светильном (коксовом) газе, а строение молекулы бензола чаще всего выражают формулой, предложенной немецким химиком А. Кекуле (1865)
Согласно современным представлениям молекула бензола имеет строение плоского шестиугольника, стороны которого равны между собой и составляют 0,14 нм. Это расстояние является средним значением между величинами 0,154 нм (длина одинарной связи) и 0,134 нм (длина двойной связи). Не только углеродные атомы, но и связанные с ними шесть атомов водорода лежат в одной плоскости. Углы, образованные связями Н-С-С и С-С-С, равны 120°:

Все углеродные атомы в молекуле бензола находятся в состоянии sр 2 -гибридизации. Каждый из них связан тремя своими гибридными орбиталями с двумя такими же орбиталями двух соседних углеродных атомов и одной орбиталью атома Н, образуя три σ-связи (см. рисунок). Четвертая, негибридизованная 2р-орбиталь атома углерода, ось которой перпендикулярна плоскости бензольного кольца, перекрывается с подобными орбиталями двух соседних углеродных атомов, расположенных справа и слева.

Схема образования σ-связей и π-связей в молекуле бензола
Такое перекрывание происходит над и под плоскостью бензольного кольца. В результате образуется единая замкнутая система π-электронов. В результате такого равномерного перекрывания 2р-орбиталей всех шести углеродных атомов происходит «выравнивание» простых и двойных связей, т.е. в бензольном кольце отсутствуют классические двойные и одинарные связи. Равномерное распределение π-электронной плотности между всеми углеродными атомами, обусловленное π-электронной делокализацией, и является причиной высокой устойчивости молекулы бензола. В настоящее время нет единого способа графического изображения молекулы бензола с учетом его реальных свойств. Но чтобы подчеркнуть выравненность π-электронной плотности в молекуле бензола, прибегают к помощи следующих формул:

Необходимо, однако, помнить, что ни одна из этих формул не отвечает действительному физическому состоянию молекулы, а тем более не может отразить все многообразие ее свойств. Формула Кекуле в настоящее время является лишь символом молекулы бензола. Однако ее широко применяют, помня при этом о ее недостатках.
Цели урока:
- дать понятие об ароматической связи, её особенностях, установить взаимосвязь между строением бензола и его свойствами;
- закрепить умение сравнивать состав и строение углеводородов различных рядов;
- познакомить с физическими свойствами бензола;
- показать токсическое воздействие аренов на здоровье человека.
План лекции
- Вывод молекулярной и структурной формулы бензола.
- История открытия бензола.
- Формула Кекуле.
- Строение бензола.
- Понятие “ароматичности”.
- Возникновение термина “ароматические соединения”.
- Физические свойства бензола.
- Токсическое воздействие аренов на организм человека.
- Закрепление пройденного материала.
- Домашнее задание.
В начале урока предлагаю учащимся решить задачу на вывод формулы вещества.
Задача. При сжигании 2,5 г вещества выделилось 8,46 г углекислого газа и 1,73 г воды. Масса 1 л вещества составляет 3,5 г. Определите молекулярную и возможную структурную формулы вещества.
Решая задачу, учащиеся выводят молекулярную формулу вещества – С 6 Н 6 . Возникает проблемная ситуация: “Какое строение может иметь молекула бензола?” Опираясь на знание о непредельных углеводородах, учащиеся предлагают возможные структурные формулы для него:
НС С-СН 2 -СН 2 - С СН
Н 2 С = СН -С С-СН = СН 2 и другие.
Учащиеся делают вывод о том, что бензол является сильно ненасыщенным соединением, вспоминают качественные реакции на непредельность.
Предлагаю учащимся проверить гипотезу о непредельности бензола в ходе выполнения эксперимента. Проведя реакции бензола с бромной водой и раствором перманганата калия, ученики приходят к выводу, что бензол, являясь ненасыщенной системой, не даёт качественных реакций на непредельность, следовательно, его нельзя отнести к классу непредельных углеводородов.
Какое же строение имеет молекула бензола, и к какому классу углеводородов его можно отнести?
Прежде, чем ответить на этот вопрос, знакомлю учеников с историей открытия бензола, которая весьма интересна. В 1812 – 1815 годах в Лондоне впервые появилось газовое освещение. Светильный газ, добывавшийся из жира морских животных, доставлялся в железных баллонах. Эти баллоны помещались обычно в подвале дома, из них газ по трубкам распределялся по всему помещению. Вскоре было замечено крайне неприятное обстоятельство – в сильные холода газ терял способность давать при горении яркий свет. Владельцы газового завода в 1825 г. обратились за советом к Фарадею, который нашёл, что те составные части, которые способны гореть ярким пламенем, собираются на дне баллона в виде прозрачного жидкого слоя. При исследовании этой жидкости Фарадей открыл новый углеводород – бензол. Название этому веществу дал Либих – (суффикс –ол указывает на его маслянистый характер, от латинского oleum – масло).
В 1865 г. немецким учёным Кекуле была предложена структура молекулы бензола, которая приснилась ему в виде змеи, укусившей себя за хвост:

Но эта формула, соответствуя элементарному составу бензола, не отвечает многим его особенностям:
- бензол не даёт качественных реакций на непредельность;
- для бензола характерны реакции замещения, а не присоединения;
- формула Кекуле не в состоянии объяснить равенства расстояний между углеродными атомами, что имеет место в реальной молекуле бензола.
Чтобы выйти из этого затруднения, Кекуле допустил, что в бензоле происходит непрерывное перемещение двойных связей.

Использование современных физических и квантовых методов исследования дало возможность создать исчерпывающее представление о строении бензола.
Атомы углерода в молекуле бензола находятся во втором валентном состоянии (sp 2). Каждый атом углерода образует -связи с двумя другими атомами углерода и одним атомом водорода, лежащими в одной плоскости. Валентные углы между тремя -связями равны 120°. Таким образом, все шесть атомов углерода лежат в одной плоскости, образуя правильный шестиугольник (рис. 1):

Рис. 1. Схема образования -связей
в молекуле бензола
Каждый атом углерода имеет одну негибридную р-орбиталь. Шесть таких орбиталей располагаются перпендикулярно плоскости -связей и параллельно друг другу (рис. 2). Все шесть р-электронов взаимодействуют между собой, образуя единое -электронное облако. Таким образом, в молекуле бензола осуществляется круговое сопряжение. Наибольшая -электронная плотность в этой сопряженной системе располагается над и под плоскостью кольца (рис. 3):
В результате такого равномерного перекрывания 2р-орбиталей всех шести углеродных атомов происходит “выравнивание” простых и двойных связей – длина связи составляет 0,139 нм. Эта величина является промежуточной между длиной одинарной связи в алканах (0,154 нм) и длиной двойной связи в алкенах (0,133 нм). То есть, в молекуле бензола отсутствуют классические двойные и одинарные связи.
Круговое сопряжение дает выигрыш в энергии 150 кДж/моль. Эта величина составляет энергию сопряжения – количество энергии, которое нужно затратить, чтобы нарушить ароматическую систему бензола.
Такое электронное строение объясняет все особенности бензола. В частности, почему бензол трудно вступает в реакции присоединения – это приводит к нарушению сопряжения. Такие реакции возможны в жёстких условиях.
В настоящее время нет единого способа графического изображения молекулы бензола с учётом его реальных свойств. Но, чтобы подчеркнуть выравненность -электронной плотности в молекуле бензола, прибегают к помощи следующих формул:

Используют и формулу Кекуле, помня при этом о её недостатках.
Совокупность свойств бензола принято называть ароматичностью. В общем виде явление ароматичности было сформулировано немецким физиком Хюккелем: соединение должно проявлять ароматические свойства, если в его молекуле содержится плоское кольцо с (4n+2) -электронами, где n может принимать значения 0, 1, 2, 3 и т. д. Согласно этому правилу, системы, содержащие 6, 10, 14 -электронов, являются ароматическими.
Примерами таких соединений являются нафталин (n=2) и антрацен (n=3).
После рассмотрения строения бензола с учащимися обсуждаем ответы на вопросы:
- Можно ли отнести бензол к непредельным углеводородам? Ответ обоснуйте.
- К какому классу углеводородов относится бензол?
- Что подразумевается под понятием “ароматическое соединение”?
- Какие углеводороды называются ароматическими?
Далее знакомлю учащихся с происхождением термина “ароматические соединения”. Сообщаю, что это название возникло в начальный период развития химии. Было замечено, что соединения бензольного ряда получаются при перегонке некоторых приятно пахнущих (ароматических) веществ – природных смол и бальзамов. Однако большинство ароматических соединений не имеют запаха или пахнут неприятно. Но данный термин сохранился в химии. Ароматическими углеводородами (аренами) называются вещества, в молекулах которых содержится одно или несколько бензольных колец – циклических групп атомов углерода с особым характером связей.
Далее учащиеся знакомятся с физическими свойствами бензола, работая с учебной литературой. Им известно, что бензол – это жидкость, может находиться и в парообразном состоянии (при исследовании запаха). Знакомлю учащихся с бензолом в твёрдом виде. Температура плавления бензола 5,5°С. Основываясь на этом сведении, демонстрирую превращение жидкого бензола в белую кристаллическую массу. Для этого 4-5 мл бензола, находящегося в пробирке, опускаю в сосуд, наполненный снегом или льдом. Через несколько минут учащиеся наблюдают изменение агрегатного состояния бензола. На основании наблюдений учащиеся высказывают предположение о том, что у этого вещества должна быть молекулярная кристаллическая решетка.
Обращаю внимание учащихся на то, что бензол является сильно токсичным веществом. Вдыхание его паров вызывает головокружение и головную боль. При высоких концентрациях бензола возможны случаи потери сознания. Его пары раздражают глаза и слизистую оболочку.
Жидкий бензол легко проникает в организм через кожу, что может привести к отравлению. Поэтому работа с бензолом и его гомологами требует особой осторожности.
Материал темы “Бензол” использую для объяснения вреда курения. Исследования дёгтеобразного вещества, полученного из табачного дыма показали, что в нём содержатся, помимо никотина, ароматические углеводороды типа бензпирена,

обладающие сильными канцерогенными свойствами, т. е. эти вещества действуют как возбудители рака. Табачный дёготь при попадании на кожу и в лёгкие вызывает образование раковых опухолей. Курильщики чаще заболевают раком губы, языка, гортани, пищевода. Они намного чаще страдают стенокардией, инфарктом миокарда. Отмечаю, что около 50% ядовитых веществ курильщик выделяет в окружающее пространство, создавая вокруг себя кольцо “пассивных курильщиков”, у которых быстро появляется головная боль, тошнота, общее недомогание, а затем могут развиваться и хронические заболевания.
В конце урока провожу фронтальный опрос по вопросам:


Домашнее задание : стр.55-58, стр. 61 №1, 2 по учебнику Э. Е. Нифантьева, Л. А. Цветкова “Химия 10-11”.
Предыдущая статья: Мемориал памяти погибших в результате чернобыльской катастрофы Следующая статья: Данные грузинской стороны
